Wurde bei Ihnen rheumatoide Arthritis diagnostiziert?
- Geschlecht Beides
- Alter 18 bis 99
- BMI 18 bis 35
- Berechnen Sie Ihren BMI hier
Wurde bei Ihnen rheumatoide Arthritis diagnostiziert?
Die Citydream-Studie zielt darauf ab, Personen wie Ihnen zu einer Linderung Ihrer Beschwerden zu verhelfen.
Wir suchen Personen mit rheumatoider Arthritis (RA), die bereit sind, an einer klinischen Studie teilzunehmen.
Rheumatoide Arthritis ist eine Autoimmunerkrankung. Bei einer Autoimmunerkrankung wendet sich das Immunsystem gegen den eigenen Körper. Bei rheumatoider Arthritis sind mehrere Gelenke oft über einen langen Zeitraum, d. h. chronisch, entzündet. Die Gelenkentzündung tritt hauptsächlich in den Händen oder Füßen auf, kann aber auch die Schulter, den Ellbogen, die Hüfte oder das Knie betreffen. Diese anhaltenden Entzündungen können dauerhafte Schäden verursachen, die zu schmerzhaften, geschwollenen und steifen Gelenken führen. Rheumatoide Arthritis kann in jedem Alter auftreten.
Welchen Zweck verfolgt die Studie?
CIT-013 ist ein neues Medikament in der Erprobungsphase, das zur Behandlung mehrerer chronischer Entzündungskrankheiten und Autoimmunerkrankungen (so auch rheumatoider Arthritis) entwickelt wird.
In dieser Studie wird untersucht, wie gut CIT-013 rheumatoide Arthritis behandelt und wie sicher dieses Medikament ist. Wir werden drei verschiedene CIT-013-Dosen mit einem Placebo vergleichen. Ein Placebo ist eine „Scheinbehandlung“ ohne Wirkstoff, die aber genauso aussieht wie das geprüfte Medikament. Weder Sie noch die Prüfärzte werden wissen, ob Sie CIT-013 oder das Placebo erhalten.
Wer kann teilnehmen?
Sie kommen eventuell für die Teilnahme infrage, wenn Sie folgende Voraussetzungen erfüllen:
- Mindestalter 18 Jahre
- Bei Ihnen wurde vor mindestens 3 Monaten rheumatoide Arthritis diagnostiziert
- Sie werden seit mindestens 3 Monaten mit einem konventionellen synthetischen krankheitsmodifizierenden Antirheumatikum (csDMARD) behandelt und sind seit mindestens 4 Wochen auf eine stabile Dosis eingestellt
- Sie haben eine mäßig aktive rheumatoide Arthritis
- Ihr Body-Mass-Index (BMI) liegt zwischen 18 und 35 kg/m².
Es gibt weitere spezifische Voraussetzungen für die Teilnahme, die Ihr Prüfarzt mit Ihnen besprechen wird.
Was geschieht, wenn Sie sich für eine Teilnahme entscheiden?
- Die Studie wird ungefähr 22 Wochen dauern;
- Sie müssen 12-mal ins Studienzentrum kommen;
- Sechs dieser Besuche werden ungefähr 2 - 2,5 Stunden dauern, die anderen sechs Besuche sind kürzer (ungefähr 1 Stunde).
Erhalten Sie eine Aufwandsentschädigung im Falle der Teilnahme an der Studie?
- Die Prüfbehandlung, die Arztbesuche, Tests und Untersuchungen sind kostenlos.
- Fahrt- oder Parkkosten in Verbindung mit dem Erscheinen zu den Terminen im Studienzentrum werden Ihnen erstattet.
So können Sie sich bewerben
Wenn Sie mehr über die Studie erfahren und wissen möchten, ob Sie für eine Teilnahme geeignet sind, registrieren Sie sich bitte auf dieser Website und beantworten Sie die folgenden Fragen. Wenn Sie in Frage kommen, wird man sich mit Ihnen in Verbindung setzen, um alle Ihre Fragen zu beantworten und einen Termin mit Ihnen zu vereinbaren.
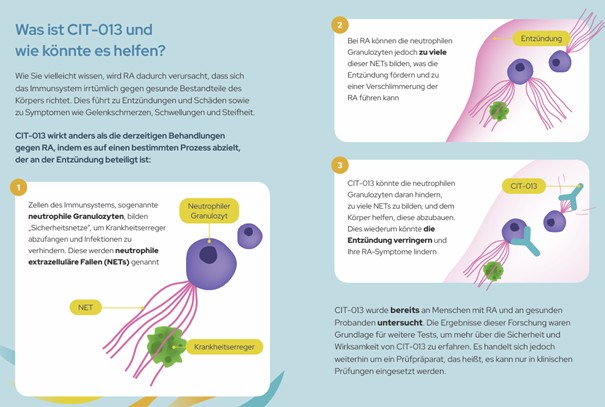
Ein gesundes Immunsystem schützt den Körper normalerweise vor Infektionen, beispielsweise durch Bakterien oder Viren. Eine Methode, den Körper vor solchen Angriffen zu schützen, besteht darin, dass Neutrophile (spezielle weiße Blutkörperchen) extrazelluläre Fallen (sogenannte NETs) produzieren, um diese
Infektionen zu bekämpfen. Bei rheumatoider Arthritis (RA) und anderen Immunerkrankungen kann es zu einer zu hohen NET-Produktion kommen, was schädlich sein kann. CIT-013 ist ein neues Medikament, das die NETs im Körper reduzieren kann. Dadurch könnten RA-bedingte Beschwerden gelindert werden. CIT-013 ist eine neue Behandlung, die anders wirkt als die derzeit für Personen mit rheumatoider Arthritis verfügbaren Behandlungen.
CIT-013 (das „Prüfmedikament“) ist noch nicht als Medikament registriert. Das Medikament wurde im Labor, an Tieren und auch an Menschen (Personen mit RA und gesunden Freiwilligen) geprüft. Obwohl CIT-013 in diesen Tests im Allgemeinen gut verträglich ist, kann es von Ärzten außerhalb von Forschungsstudien noch nicht verschrieben werden. Das liegt daran, dass wir noch überprüfen müssen, ob CIT-013 eine wirksame Behandlung für RA ist.
Diese Studie erfordert, dass Sie häufiger ins Studienzentrum kommen müssen als zu Ihren üblichen Rheumatologie-Terminen. Während der Termine werden außerdem mehr Untersuchungen durchgeführt (wie zuvor beschrieben), um Ihre Gesundheit während der gesamten Studie zu überwachen.
In den meisten Fällen können Sie die gewohnte Behandlung Ihrer rheumatoiden Arthritis während der Studie fortsetzen.
Schritt 1:
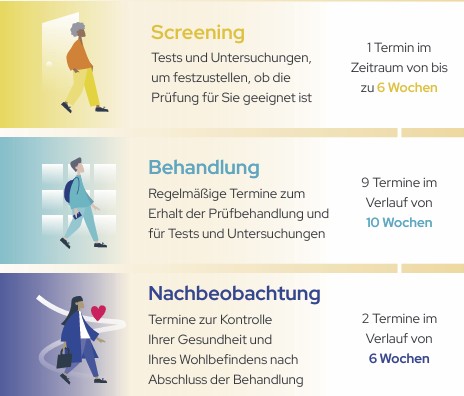
Voruntersuchung (Screening): Kommen Sie für eine Teilnahme in Frage?
Der Prüfarzt wird einige Überprüfungen durchführen:
Schritt 2:
Die Behandlung mit dem Placebo oder dem Prüfmedikament (Behandlungszeitraum 1)
Vor der Gabe des Prüfmedikaments wird die ärztliche Untersuchung (siehe Schritt 1) wiederholt.
Im ersten Teil der Behandlung erhalten Sie 6 Wochen lang das Prüfmedikament oder das Placebo. Sie erhalten alle zwei Wochen 1 Dosis, also insgesamt drei Dosen während des Behandlungszeitraums 1. Das Prüfmedikament und das Placebo werden Ihnen am Bauch unter die Haut gespritzt.
Schritt 3:
Die Behandlung mit 50 mg des Prüfmedikaments (Behandlungszeitraum 2)
Nach dem Behandlungszeitraum 1 erhalten alle Teilnehmenden 6 Wochen lang 50 mg des Prüfmedikaments. Sie erhalten alle zwei Wochen 1 Dosis, also insgesamt drei Dosen während des Behandlungszeitraums 2.
Schritt 4:
Nachuntersuchung
Es werden zwei Nachuntersuchungen durchgeführt, um Ihre Gesundheit nach den Behandlungszeiträumen zu überprüfen.
Bei der ärztlichen Untersuchung in Schritt 2, 3 und 4 werden hauptsächlich folgende Verfahren durchgeführt:
Untersuchung der Krankheitsaktivität. Ihre Gelenke werden auf Schwellungen und Druckempfindlichkeit untersucht. Der Prüfarzt wird maximal 11 Röhrchen Blut auf einmal abnehmen. Insgesamt entnehmen wir Ihnen etwa 260 ml Blut. Sie müssen während der Studie fünfmal einen Fragebogen beantworten.
Die Teilnahme an einer klinischen Studie ist vollkommen freiwillig und hat keinen Einfluss auf Ihre normale medizinische Versorgung.
Was geschieht, wenn Sie sich für eine Teilnahme entscheiden?
Klinische Forschung hilft Ärzten und Wissenschaftlern festzustellen, ob ein Prüfmedikament oder eine Prüftherapie bei der Anwendung beim Menschen zur potenziellen Behandlung eines Leidens, einer Krankheit oder einer Störung unbedenklich/sicher bzw. wirksam ist. Bei klinischen Studien ist es häufig notwendig, dass viele Freiwillige an einer einzelnen Studie teilnehmen, und manchmal sind Tausende erforderlich, um zuverlässige Informationen zu erhalten.
Was ist eine informierte Einwilligung?
Die „informierte Einwilligung“ ist ein Prozess der Informationsübermittlung, bevor eine erwachsene Person zustimmt, an einem Forschungsvorhaben teilzunehmen. Potentielle Studienteilnehmende werden gebeten, eine Teilnehmerinformation und Einwilligungserklärung zu lesen und zu unterzeichnen, erhalten aber auch mündliche und schriftliche Informationen und anderes Material zum Durchlesen. Sie haben darüber hinaus immer wieder die Möglichkeit, Fragen zu stellen, die beantwortet werden, damit sichergestellt ist, dass die/der potenzielle Studienteilnehmende die Studie versteht und sich aus freien Stücken für die Teilnahme entscheidet.
Bevor Sie sich bereit erklären, freiwillig an der Studie teilzunehmen, muss der Studienarzt oder ein/e Studienmitarbeitende/r Ihnen alle Einzelheiten der Studie, einschließlich der Risiken und Vorteile, erklären und Ihre Fragen beantworten. Nachdem alle Ihre Fragen beantwortet wurden und wenn Sie teilnehmen möchten, unterzeichnen Sie eine so genannte „Einwilligungserklärung“, mit der Sie Folgendes bestätigen:
Sie erklären sich bereit, freiwillig teilzunehmen. Sie verstehen die Studie, einschließlich ihres Ablaufs, ihrer Risiken und möglicher Nebenwirkungen des Prüfmedikaments. Ihnen ist bewusst, dass Sie jederzeit und aus jedem Grund aus der Studie ausscheiden können.Wenn Sie nicht verstehen, was von Ihnen erwartet wird oder was in dem Dokument steht, sollten Sie weitere Fragen stellen und mit dem Studienarzt, Ihrer Familie oder anderen Personen Ihres Vertrauens sprechen, bis Sie das Gefühl haben, alles verstanden zu haben.

 Argentina
Argentina Australia
Australia Balgarija
Balgarija België
België Canada
Canada Česko
Česko Chile
Chile China (中国)
China (中国) Colombia
Colombia Danmark
Danmark Deutschland
Deutschland England
England España
España France
France Ireland
Ireland Italiana
Italiana Lietuva
Lietuva Magyarország
Magyarország Nederland
Nederland New Zealand
New Zealand Österreich
Österreich Polska
Polska Schweiz
Schweiz Singapore
Singapore Slovenija
Slovenija Slovensko
Slovensko Suomi
Suomi Sverige
Sverige United States
United States Israel
Israel